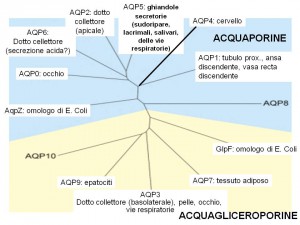
Le acquaporine sono espressi in molti tessuti
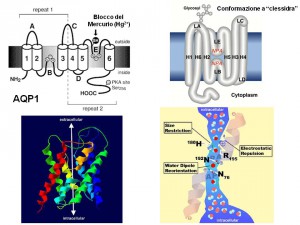
La struttura delle Acquaporine è così caratterizzata:
- 6 domini transmembrana con entrambe le estremita’ intracellulari
- Motivo specifico per le acquaporine : NPA , nei lops B ed E
- Loops B ed E formano il poro che permette il passaggio dell’acqua
- Struttura tetramerica, ogni monomero forma un poro funzionalmente permeabile all’acqua.
- La permeabilita’ selettiva all’acqua è dovuta a legami elettrostatici creati da ciascun lato del poro
- Le 2 asparagine dei motivi NPA creano un ambiente idrofilico in cui l’acqua forma legami idrogeno , ruota di 180˚
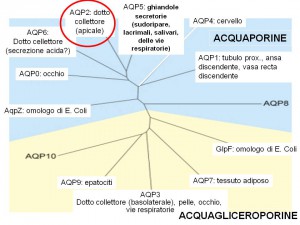
Regolazione dell’espressione dell’AQP2:il ruolo della vasopressina
- La permeabilità dell’acqua è regolata dalla presenza del canale dell’acqua AQP2, la cui espressione è modulata dalla vasopressina
- Il rilascio della vasopressina, da parte dei nuclei sopraottico e paraventricolare dell’ipotalamo, avviene in risposta ad un incremento dell’osmolarità plasmatica o riduzione della volemia
- Viene stimolato il riassorbimento dell’H20 attraverso una traslocazione delle vescicole contenenti l’acquaporina 2 sulla membrana apicale (meccanismo di “Shuttle di membrana”)
Regolazione AQP2
- ADH-dipendente
- ADH-indipendente
In esperimenti col litio si dimostrava una profonda downregulation di AQP2, con poliuria massiva( inibizione AC con riduzione cAMP)
Ossitocina (rec. V2), insulina,PGE2,dopamina
- Regolazione “ short-term”: traffico di ACQ2 tra vescicole intracellulari e membrana apicale (ADH, ossitocina)
- Regolazione “long-term”: cambiamenti nel numero totale di canali, ( livello tracrizionale/turnover proteico) escape da ADH
Meccanismo d’azione della vasopressina sulla traslocazione dell’AQP
Attivazione della proteina PKA
- La PKA è una proteina multimerica, costituita da 2 subunità catalitiche e 2 regolatrici
- L’AMPc lega le subunità regolatrici dissociandole da quelle catalitiche con conseguente attivazione della proteina PKA
- La PKA ora attiva, fosforila molte proteine cellulari, tra cui l’AQP2, che trasloca verso la membrana apicale,incrementando la permeabilità all’H2O
- E’ nota la presenza di un sito di consenso per la PKA nell’AQP2 in corrispondenza della Ser-256 presente nel dominio COOH-terminale della proteina
Dinamiche del citoscheletro nella traslocazione dell’AQP2
- Queste consentono alla cellula di regolare la forma e il volume in risposta a stimoli esterni e a variazioni della composizione ionica dello spazio intra ed extra cellulare
- Rho media infatti la formazione delle fibre “da stress” che rappresentano le strutture filamentose dello scheletro di actina
- Le proteine della famiglia Rho partecipano alla regolazione del meccanismo di traslocazione delle vescicole del pathway esocitico attraverso la modulazione dello stato di polimerizzazione del citoscheletro di actina
- Quando la vasopressina, legandosi al recettore V2, porta ad un incremento di AMPc stimolando così l’attivazione della PKA, si ha anche la fosforilazione della RhoA in corrispondenza della Ser-188
- Dineina e dinactina , un complesso proteico che si pensa medi l’interazione della dineina con le vescicole ,si ritiene siano coinvolte nel traffico delle vescicole di trasporto dell’AQP2
- Gli inibitori di tali sistemi, infatti, inibiscono la risposta antidiuretica
- La parte apicale delle cellule del collettore contiene un prominente apparato di filamenti di actina che sembra siano coinvolti nella risposta idroosmotica , visto che la distruzione dei microfilamenti inibisce la risposta antidiuretica
- I microfilamenti sono probabilmente coinvolti nel movimento finale delle vescicole, nella loro fusione con la membrana plasmatica e con la successiva endocitosi dei canali dell’acqua. La vasopressina causa da sola la depolarizzazione dell’actina , suggerendo che la riorganizzazione di questa struttura sia una parte importante della risposta cellulare alla vasopressina
- E’ possibile che un apparato molecolare simile al sistema SNARE (soluble NSF attachment protein receptors) sia presente nelle cellule principali del collettore . Secondo tale ipotesi vi sarebbero specifiche proteine sulle vescicole (vSNAREs) e sulla membrana plasmatica target (tSNAREs) che interagiscono con i componenti di un complesso di fusione per indurre la fusione delle vescicole solo con la richiesta membrana target.
- L’inserzione dell’AQP2 serebbe controllata da proteine simili a quelle coinvolte nella trasmissiono sinaptica
Per Concludere:
- In condizioni basali, l’AQP2 presente nelle vescicole citoplasmatiche è in parte fosforilata. Questo evento,tuttavia, in assenza di stimolazione ormonale, non è sufficiente per la sua traslocazione sulla membrana apicale
- La traslocazione della AQP2 avviene solo se vengono fosforilati almeno tre dei monomeri che costituiscono il tetramero di AQP2 in corrispondenza del residuo di serina in posizione 256
- La fosforilazione dell’AQP2 nel rene non incrementa la permeabilità del canale dell’acqua ma è determinante nel processo di regolazione del traffico vescicolare verso la membrana
- La fosforilazione dell’AQP2 regolata dalla PKA non è l’unico responsabile della traslocazione del canale verso la membrana apicale delle cellule principali. Intervengono infatti altri meccanismi che coinvolgono altre proteine con processi molecolari ben più complessi
Patologie associate alle acquaporine
Diabete insipido
Parole chiave: ADH ( ipotalamo); recettoreV2( membrana basolaterale cellule collettore); aumento permeabilita’ transepiteiale all’acqua
- Centrale ( manca ADH ); ( ridotta espressione di AQP2)
- Nefrogenico di tipo Congenito
- X-linked ( gene del rec V2)
- Autosomico recessivo ( gene AQP2)
Diabete insipido nefrogenico Acquisito
RIDOTTA ESPRESSIONE DI AQP2
- Ipokaliemia
- Ipercalcemia
- Ostruzione bilaterale delle vie urinarie
- Litio
Insufficienza renale terminale
- Fine et al. hanno osservato che dotti collettori isolati e perfusi da reni di ratti con uremia severa avevano una riduzione significativa del flusso dell’acqua e delll’attivita’ dell’adenilato ciclasi in risposta all’ADH
- Nei reni di ratti con IRC è stata rivelata assenza virtuale di mRNA per il recettore V2
- In modelli di ratto con IRC è stata osservata ridotta espressione di AQP2 e AQP3 e una downregulation dell’ AQP2 resistente all’ADH
- Il rilascio non osmotico di ADH interviene in diverse condizioni, tra cui gravidanza, cirrosi e scompenso cardiaco congestizio ( CHF), per alterazione della circolazione arteriosa dovuta, nei primi due casi, al rilascio di NO
- Il rilascio non osmotico di ADH, mediato dai barocettori, ma anche da endotelina, prostaglandine, angiotensina,sembra giocare un ruolo determinante nel CHF
Scompenso cardiaco
Il cuore è incapace di soddisfare le richieste dei tessuti periferici
Il rene ritiene acqua e sodio, nonostante l’espansione del volume extracellulare
- Percezione di inadeguato volume circolante da parte dei sensori
- Eccessiva attivazione dei sistemi di vasocostrizione( antinatriuretici) e insufficienza dei meccanismi vasodilatatori (natriuretici)
- Insufficienza retrograda: l’accumulo di sangue a monte del miocardio insufficiente esita in congestione venosa, aumento della pressione capillare e trasudazione nell’interstizio, con diminuzione del volume plasmatico
- Insufficienza anterograda: insufficienza della pompa cardiaca e flusso inadeguato ai tessuti, tra cui il rene
“UNDERFILLING”
- Riflessi cardiopolmonari e barocettoriali attenuati
- Resistenza all’ ANP
- Aumento delle resistenze vascolari con aumento della FF
- Iperattivita’ del SRAA e del SNA
- Aumento dell’ET ( aumento resistenze vascolari)
- Riduzione della vasodilatazione endotelio-dipendente
- Un aumento mediato dai barocettori del rilascio di ADH si pensa abbia un ruolo critico per la ritenzione di acqua e lo sviluppo dell’iponatriemia nel CHF
Modello di scompenso cardiaco con legatura della coronaria sinistra
lo scompenso cardiaco congestizio con ritenzione renale di acqua (sviluppo di iponatriemia) era associato con un marcato aumento dell’mRNA dell’ AQP2 e aumentata distribuzione di AQP2 a livello della membrana apicale.I livelli di AQP1 e 3 restavano invariati
Ratti con scompenso cardiaco congestizio avevano livelli significativamente aumentati di ADH e la somministrazione dell’antagonista del recettore V2 per l’ADH (OPC 31260 ) era associata a significativa riduzione dei livelli di AQP2
Nel CHF sperimentale del ratto il ruolo maggiore nell’upregulation dell’ AQP2 è svolto dall’ADH
In pazienti con scompenso cardiaco classe NYHA II o III, l’antagonista del recettore V2 causava una diuresi di acqua ( solute-free ) e aumentava la concentrazione plasmatica di sodio, con conseguente perdita di peso
Cirrosi
- Underfilling: vasodilatazione periferica e conseguente deplezione del compartimento intravascolare arterioso
- Overflow: ritenzione renale di sodio non volume-dipendente come alterazione primitiva nelle fasi precoci della cirrosi
- La vasopressina è aumentata nella cirrrosi per stimolazione non osmotica
- Nella cirrosi epatica indotta da somministrazione cronica intraperitoneale di CCl4 si è assistito ad aumentata espressione di AQP2 mRNA (in tali modelli tuttavia i ratti avevano normali livelli di sodio sierico o osmolalità, indicando che l’inappropriata ritenzione renale di acqua non era il fattore principale nella genesi dell’ascite)
- livelli di mRNA di AQP2 correlavano con la quota di ascite . Il trattamento con l’antagonista del recettore V2 (OPC31260) rendeva reversibile l’aumento dei livelli di AQP2
- Un secondo modello di cirrosi (compensata) è indotto con la legatura del dotto biliare comune. L’ immunoblotting e la densitometria semiquantitativa hanno dimostrato una riduzione significativa dell’espressione di AQP2; a cio’ si aggiungeva la dimostrazione di un ridotto effetto del trattamento con antagonista del recettoreV2
- In un terzo modello, con inalazione di CCl4, la cirrosi si associava ad ascite e iponatriemia, ma non si osservavano variazioni del’espressione di AQP2 mentre l’espressione di AQP1 nella corticale era aumentata
- la downregulation of AQP2 osservata in forme moderate di cirrosi (es., in uno stadio compensato senza ritenzione di acqua) potrebbe rappresentare un meccanismo compensatorio per prevenire lo sviluppo di ritenzione,mentre i livelli elevati di ADH osservati nella cirrosi severa, non compensata, con ascite, possono indurre un’inappropriata upregulation di AQP2 che potrebbe essere coinvolta nello sviluppo di ritenzione di acqua
Gravidanza
Underfilling
( vasodilatazione periferica)
- Il rilascio non osmotico di ADH, secondario alla vasodilatazione arteriosa, è coinvolto nella ritenzione idrica in gravidanza
- In ratti gravidi, c’è anche un aumento dell’ACQ2 nelle membrane, indicando un aumento del “trafficking” di ACQ2 alla membrana apicale
- La somministrazione di antagonisti del recettore V2 , sopprimeva l’aumento di mRNA di AQP2 e dunque di AQP2Presenza di fattori indipendenti dall’ADH (es. effetto antidiuretico dell’ossitocina mediato dal recettore V2 )
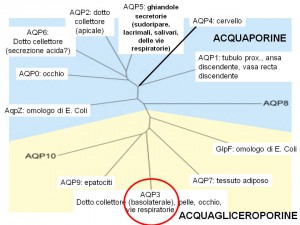
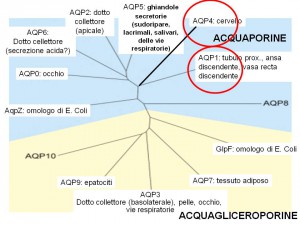
Acquagliceroporine
- Gruppo di AQP che oltre a trasportare acqua, veicola anche glicerolo
- AQP3 ha un ruolo essenziale nell’idratazione dell’epidermide, creando un circuito di acqua fra lo stato basale e lo strato corneo al fine di garantire un mantenimento idrico costante
- Il trasporto di acqua AQP3-mediato è PH sensibile, se il PH scende da 7 a 4, il trasporto si blocca.
- Nell’ epidermide, la presenza di AQP3 e il PH 7 assicurano il movimento di acqua
- L’assenza di AQP3 e il PH 5 impediscono la perdita di acqua
- I risultati ottenuti con esperimenti su topi Knockout in AQP3, hanno permesso di ipotizzare che la corretta idratazione della pelle sia assicurata dalla capacita’ delle AQP3 di trasportare anche il glicerolo oltre che l’acqua
- I topi Knockout in AQP3 infatti manifestano anomalie fenotipiche, quali la ridotta idratazione ed elasticità della pelle, ritardo nella biosintesi dello strato corneo dopo stripping e riparo delle ferite, corrette poi mediante somministrazione di glicerolo per via sistemica o topica
- Il glicerolo nell’epidermide eserciterebbe oltre alla nota capacità umettante, anche un ruolo biosintetico come precursore dei lipidi, molecole segnale: fostatidilglicerolo (regolatore della proliferazione e del differenziamento dei cheratinociti)
Il ruolo delle AQP1 e AQP4 nelle fasi iniziali della malattia di Alzheimer
- Recenti studi hanno dimostrato la presenza di un espressione alterata di AQP1 negli astrociti, durante le fasi iniziali della malattia di Alzheimer, determinando un alterato controllo di flussi di acqua proprio in queste cellule.
- Durante le fasi iniziali della malattia, si osservano un rigonfiamento seguito da un aumento delle vescicole di pinicitosi nelle cellule endoteliali, atrofia e alterazioni delle fibre muscolari lisce, addensamento e rigonfiamento delle estroflessioni degli astrocitiGli astrociti sono forniti di numerose estroflessioni che ancorano i neuroni contribuendo al nutrimento
- Essi si dividono in astrociti protoplasmatici, presenti nella sostanza grigia e caratterizzati dalla presenza di espansioni corte, e astrociti fibrosi, presenti nella sostanza bianca e caratterizzati da prolungamenti citoplasmatici lunghi e sottili. Regolano l’ambiente chimico esterno dei neuroni rimuovendo gli ioni, in particolare il potassio, e riciclano i neurotrasmettitori rilasciati durante la trasmissione sinaptica e sono responsabili dei meccanismi di vasocostrizione e vasodilatazione producendo sostanze vasoattivi come l’acido arachidonico
- Le AQP1 sono espresse negli astrociti in particolare nelle loro estroflessioni che prendono contatto diretto con i neuroni.
- Possono essere espresse anche in particolari condizioni quali edema cerebrale da trauma cranico.
- L’AQP4 è l’acquaporina predominante nel tessuto cerebrale espressa oltre che negli astrociti anche nelle cellule ependimali che delimitano le cavità del sistema nervoso centrale e, col battito delle ciglia favoriscono la circolazione del liquido cerebrospinale.
- Il ruolo dell’AQP4 nell’edema cerebrale è confermato dagli studi di Amyry-Moghaddam che hanno dimostrato la risoluzione del fenomeno mediante delezione di AQP4
- Quindi le alterazioni degli astrociti, delle cellule endoteliai: perdita di actina nelle nella muscolatura liscia, di collagene di tipo IV, eparansolfato e proteoglicano, determinano disgregazione della membrana basale.
- Queste anomalie contribuiscono all’insorgenza di patologie cerebrovascolari che insieme alla formazione della placca senile, alle mutazioni Preseniline (PS-1;PS-2) e all’iperfosforilazione della prtoteina Tau, cotribuiscono al complesso quadro patologico della Malattia di Alzheimer
Il ruolo dell’AQP1 nell’angiogenesi tumorale
- L’angiogenesi è un processo vitale per la crescita dei tumori solidi, recenti studi (Nature, Saadoun et al) hanno dimostrato che nei topi con delezione della proteina AQP1, hanno una ridotta angiogenesi tumorale.
- Gli studi hanno dimostrato una up-regulation per il gene dell’AQP1 da parte degli estrogeni.
- Qual è il ruolo del trasporto dell’acqua nell’angiogenesi tumorale?
- Il lavoro di Saadoun ha mostrato che la delezione dell’AQP1, riduce la migrazione delle cellule endoteliali senza alterazione della proliferazione e adesione.
- Il processo di migrazione delle cellule endoteliali rappresenta il primo passo nell’angiogenesi ed è collegato alla permeabilità vascolare.
- L’incremento della permeabilità vascolare, è necessario per attivare le cellule endoteliali a partecipare alla cascata dell’ angiogenesi (fuoriuscita di proteine plasmatiche sul versante extravasale che rappresentano una sorta di ponteggio provvisorio per la migrazione delle cellule endoteliali)
- La scoperta che un aumentato trasporto di acqua contribuisca alla migrazione delle cellule endoteliali (grazie alle proprietà osmotiche dell’acqua), sembra attribuire all’AQP1 un ruolo fondamentale nelle patologie caratterizzate da un aumentata permeabilitè endoteliale come nell’angiogenesi tumorale.
BIBLIOGRAFIA:
- Agre P, Preston GM, Smith BL, Jung JS, Raina S, Moon C, Guggino WB, and Nielsen S. Aquaporin CHIP: the archetypal molecular water channel. Am J Physiol Renal Fluid Electrolyte Physiol 265: F463-F476, 1993
- Agre P, Saboori AM, Asimos A, and Smith BL. Purification and partial characterization of the Mr 30,000 integral membrane protein associated with the erythrocyte Rh (D) antigen. J Biol Chem 262: 17497-17503, 1987
- Preston GM, and Agre P. Isolation of the cDNA for erythrocyte integral membrane protein of 28 kilodaltons: member of an ancient channel family. Proc Natl Acad Sci USA 88: 11110-11114, 1991
- Preston GM, Carroll TP, Guggino WB, and Agre P. Appearance of water channels in Xenopus oocytes expressing red cell CHIP28 protein. Science 256: 385-387, 1992
- Saboori AM, Smith BL, and Agre P. Polymorphism in the Mr 32,000 Rh protein purified from Rh (D)-positive and -negative erythrocytes. Proc Natl Acad Sci USA 85: 4042-4045, 1988
- Wright EM, Hediger MA, Coady MJ, Hirayama B, and Turk E. Molecular biology of Na+/glucose cotransport. Biochem Soc Trans 17: 810-811, 1989
- The renal plumbing system: aquaporin water channels, CMLS 62 (2005)192-1706
- -Walz T, Hirai T, Murata K, Heymann JB, Mitsuoka K, Fujiyoshi Y, Smith BL, Agre P, and Engel A. The three-dimensional structure of aquaporin-1. Nature 387: 624-627, 1997
- Walz T, Smith BL, Agre P, and Engel A. The three-dimensional structure of human erythrocyte aquaporin CHIP. EMBO J 13: 2985-2993, 1994
- Walz T, Tittmann P, Fuchs KH, Muller DJ, Smith BL, Agre P, Gross H, and Engel A. Surface topographies at subnanometer-resolution reveal asymmetry and sidedness of aquaporin-1. J Mol Biol 264: 907-918, 1996
- Li H, Lee S, and Jap BK. Molecular design of aquaporin-1 water channel as revealed by electron crystallography. Nat Struct Biol 4: 263-265, 1997
- Cheng A, Van HA, Yeager M, Verkman AS, and Mitra AK. Three-dimensional organization of a human water channel. Nature 387: 627-630, 1997
- Boton R, Gaviria M, and Batlle DC. Prevalence, pathogenesis, and treatment of renal dysfunction associated with chronic lithium therapy. Am J Kidney Dis 10: 329-345, 1987
- Christensen S, Kusano E, Yusufi AN, Murayama N, and Dousa TP. Pathogenesis of nephrogenic diabetes insipidus due to chronic administration of lithium in rats. J Clin Invest 75: 1869-1879, 1985
- Knepper MA: Molecular physiology of urinary concentrating mechanism: Regulation of aquaporin water channels by vasopressin. Am J Physiol 272: F3-F12,1997 e: CMLS 62,2005, 1692-1706
- Valenti G, Procino G, Carmosino M, Frigeri A, Mannucci R, Nicoletti I, Svelto M.The phosphatase inhibitor okadaic acid induces AQP2 translocation independently from AQP2 phosphorylation in renal collecting duct cells.J Cell Sci. 2000 Jun;113 ( Pt 11):1985-92.
- Procino G, Carmosino M, Marin O, Brunati AM, Contri A, Pinna LA, Mannucci R, Nielsen S, Kwon TH, Svelto M, Valenti G.Ser-256 phosphorylation dynamics of Aquaporin 2 during maturation from the ER to the vesicular compartment in renal cells.FASEB J. 2003 Oct;17(13):1886-8. Epub 2003 Aug 1.
- Cho MR, Knowles DW, Smith BL, Moulds JJ, Agre P, Mohandas N, Golan DE. Membrane dynamics of the water transport protein aquaporin-1 in intact human red cells.Biophys J. 1999 Feb;76(2):1136-44.
- Maekawa M, Ishizaki T, Boku S, Watanabe N, Fujita A, Iwamatsu A, Obinata T, Ohashi K, Mizuno K, Narumiya S.Signaling from Rho to the actin cytoskeleton through protein kinases ROCK and LIM-kinase.Science. 1999 Aug 6;285(5429):895-8.
- Marples D, Schroer TA, Ahrens N, Taylor A, Knepper MA, Nielsen S: Dynein and dynactin colocalize with AQP2 water channels in intracellular vesicles from kidney collecting duct. Am J Physiol274 : F384-F394,1998
- de-Sousa RC, Grosso A: Vanadate blocks cyclic AMP-induced stimulation of sodium and water transport in amphibian epithelia.Nature 279:803 -804, 1979
- Marples D, Barber B, Taylor A: Effect of a dynein inhibitor on vasopressin action in toad urinary bladder. J Physiol Lond490 : 767-774,1996
- Wade JB, Kachadorian WA: Cytochalasin B inhibition of toad bladder apical membrane responses to ADH. Am J Physiol255 : C526-C530,1988
- Pearl M, Taylor A: Actin filaments and vasopressin-stimulated water flow in toad urinary bladder. Am J Physiol245 : C28-C39,1983
- Kachadorian WA, Ellis SJ, Muller J: Possible roles for microtubules and microfilaments in ADH action on toad urinary bladder. Am J Physiol 236: F14-F20,1979
- Muller J, Kachadorian WA: Aggregate-carrying membranes during ADH stimulation and washout in toad bladder. Am J Physiol247 : C90-C98,1984 Pearl M, Taylor A: Role of the cytoskeleton in the control of transcellular water flow by vasopressin in amphibian urinary bladder.Biol Cell 55:163 -172, 1985
- Ding GH, Franki N, Condeelis J, Hays RM: Vasopressin depolymerizes F-actin in toad bladder epithelial cells. Am J Physiol260 : C9-C16,1991
- DiBona DR: Cytoplasmic involvement in ADH-mediated osmosis across toad urinary bladder. Am J Physiol 245:C297 -C307, 1983
- Rothman JE: Mechanisms of intracellular protein transport.Nature 372:55 -63, 1994
- Rothman JE: Mechanisms of intracellular protein transport.Nature 372:55 -63, 1994
- Nielsen S, Marples D, Birn H, Mohtashami M, Dalby NO, Trimble M, Knepper M: Expression of VAMP-2-like protein in kidney collecting duct intracellular vesicles: Co-localization with aquaporin-2 water channels.J Clin Invest 96:1834 -1844, 1995
- Franki N, Macaluso F, Gao Y, Hays RM: Vesicle fusion proteins in rat inner medullary collecting duct and amphibian bladder. Am J Physiol 268: 792-797,1995
- Jo I, Harris HW, Amedt-Raduege AM, Majewski RR, Hammond TG: Rat kidney papilla contains abundant synaptobrevin protein that participates in the fusion of antidiuretic hormone (ADH) water channel-containing endosomes in vitro. Proc Natl Acad Sci USA 92:1876 -1880, 1995
- Mandon B, Chou CL, Nielsen S, Knepper MA: Syntaxin-4 is localized to the apical plasma membrane of rat renal collecting duct cells: Possible role in aquaporin-2 trafficking. J Clin Invest98 : 906-913,1996
- Mandon B, Nielsen S, Kishore BK, Knepper MA: Expression of syntaxins in rat kidney. Am J Physiol273 : F718-F730,1997
- Nishimoto G, Zelenina M, Li D, Yasui M, Aperia A, Nielsen S, Nairn AC.Arginine vasopressin stimulates phosphorylation of aquaporin-2 in rat renal tissue.Am J Physiol. 1999 Feb;276(2 Pt 2):F254-9
- BRENNER, “IL RENE”, 6 ED.
- DiGiovanni SR, Nielsen S, Christensen EI, Knepper MA: Regulation of collecting duct water channel expression by vasopressin in Brattleboro rat.Proc Natl Acad Sci USA 91:8984 -8988, 1994
- Fine LG, Schlondorff D, Trizna W, Gilbert RM, Bricker NS: Functional profile of the isolated uremic nephron: Impaired water permeability and adenylate cyclase responsiveness of the cortical collecting tubule to vasopressin. J Clin Invest 61:1519 -1527, 1978
- Teitelbaum I, McGuinness S: Vasopressin resistance in chronic renal failure: Evidence for the role of decreased V2 receptor mRNA. J Clin Invest 96: 378-385,1995
- Goldfine ID: Interaction of insulin, polypeptide hormones, and growth factors with intracellular membranes. Biochim Biophys Acta 650: 53-67,1981
- Kwon TH, Frøkiær J, Knepper MA, Nielsen S: Reduced AQP1, -2, and -3 levels in kidneys of rats with CRF induced by surgical reduction in renal mass. Am J Physiol275 : F724-F741,1998
- Fine LG, Schlondorff D, Trizna W, Gilbert RM, Bricker NS: Functional profile of the isolated uremic nephron: Impaired water permeability and adenylate cyclase responsiveness of the cortical collecting tubule to vasopressin. J Clin Invest 61:1519 -1527, 1978
- Teitelbaum I, McGuinness S: Vasopressin resistance in chronic renal failure: Evidence for the role of decreased V2 receptor mRNA. J Clin Invest 96: 378-385,1995
- Goldfine ID: Interaction of insulin, polypeptide hormones, and growth factors with intracellular membranes. Biochim Biophys Acta 650: 53-67,1981
- Kwon TH, Frøkiær J, Knepper MA, Nielsen S: Reduced AQP1, -2, and -3 levels in kidneys of rats with CRF induced by surgical reduction in renal mass. Am J Physiol275 : F724-F741,1998
- Recent advances in the understanding of water metabolism in heart failure, Schrier R.H., Martin P.Y. , Adv Exp Med Biol. 1998, (449): 415-426
- Recent advances in the understanding of water metabolism in heart failure, Schrier R.H., Martin P.Y. , Adv Exp Med Biol. 1998, (449): 415-426
- Fujita N, Ishikawa SE, Sasaki S, Fujisawa G, Fushimi K, Marumo F, Saito T: Role of water channel AQP-CD in water retention in SIADH and cirrhotic rats. Am J Physiol 269:F926 -F931, 1996
- Asahina Y, Izumi N, Enomoto N, Sasaki S, Fushimi K, Marumo F, Sato C: Increased gene expression of water channel in cirrhotic rat kidneys.Hepatology 21:169 -173, 1995
- Jonassen T, Nielsen S, Christensen S, Petersen JS: Decreased vasopressin-mediated renal water reabsorption in rats with compensated liver cirrhosis. Am J Physiol 275:F216 -F225, 1998
- Fernandez-Llama P, Jimenez W, Bosch-Marce M, Arroyo V, Nielsen S, Knepper MA: Dysregulation of aquaporin-1 and aquaporin-2 in the kidneys of cirrhotic rats [Abstract]. J Am Soc Nephrol9 : 18a,1998
- Aquaporins in the Kidney: From Molecules to Medicine , Søren Nielsen, Jørgen Frøkiær, David Marples, Tae-Hwan Kwon, Peter Agre, and Mark A. Knepper .Physiol. Rev. 82: 205-244, 2006
- Body Water Homeostasis: Clinical Disorders of Urinary Dilution and Concentration , Robert W. Schrier J Am Soc Nephrol 17: 1820-1832, 2006
- Schrier RW, Ohara M, Rogachev B, Xu L, and Knotek M. Aquaporin-2 water channels and vasopressin antagonists in edematous disorders. Mol Genet Metab 65: 255-263, 1998
- Boury-Jamot M, Sougrat R, Tailhardat M, Le Varlet B, Bonté F, Dumas M, Verbavatz JM.Expression and function of aquaporins in human skin: Is aquaporin-3 just a glycerol transporter?Biochim Biophys Acta. 2006 Aug;1758(8):1034-42. Epub 2006 Jun 18.
- Boury-Jamot M, Sougrat R, Tailhardat M, Le Varlet B, Bonté F, Dumas M, Verbavatz JM.Expression and function of aquaporins in human skin: Is aquaporin-3 just a glycerol transporter?Biochim Biophys Acta. 2006 Aug;1758(8):1034-42. Epub 2006 Jun 18.
- Choi EH, Man MQ, Wang F, Zhang X, Brown BE, Feingold KR, Elias PM.Is endogenous glycerol a determinant of stratum corneum hydration in humans?J Invest Dermatol. 2005 Aug;125(2)
- Pérez E, Barrachina M, Rodríguez A, Torrejón-Escribano B, Boada M, Hernández I, Sánchez M, Ferrer I. Aquaporin expression in the cerebral cortex is increased at early stages of Alzheimer disease.Brain Res. 2007 Jan 12;1128(1):164-74. Epub 2006 Nov 22.
- Farkas E, Luiten PG. Cerebral microvascular pathology in aging and Alzheimer’s disease.Prog Neurobiol. 2001 Aug;64(6):575-611. Review.
- Amiry-Moghaddam M, Ottersen OP.The molecular basis of water transport in the brain.Nat Rev Neurosci. 2003 Dec;4(12):991-1001.
- Amiry-Moghaddam M, Williamson A, Palomba M, Eid T, de Lanerolle NC, Nagelhus EA, Adams ME, Froehner SC, Agre P, Ottersen OP.Delayed K+ clearance associated with aquaporin-4 mislocalization: phenotypic defects in brains of alpha-syntrophin-null mice.Proc Natl Acad Sci U S A. 2003 Nov 11;100(23):13615-20. Epub 2003 Nov 3.
- Bertram L, Tanzi RE. Alzheimer’s disease: one disorder, too many genes?Hum Mol Genet. 2004 Apr 1;13 Spec No 1:R135-41. Epub 2004 Feb 5. Review.
- Kalaria RN, Pax AB.Increased collagen content of cerebral microvessels in Alzheimer’s disease.Brain Res. 1995 Dec 24;705(1-2):349-52.
- Kalaria RN, Hedera P.Differential degeneration of the cerebral microvasculature in Alzheimer’s disease.Neuroreport. 1995 Feb 15;6(3):477-80.
- Verbeek MM, Otte-Höller I, van den Born J, van den Heuvel LP, David G, Wesseling P, de Waal RM.Agrin is a major heparan sulfate proteoglycan accumulating in Alzheimer’s disease brain.Am J Pathol. 1999 Dec;155(6):2115-25.
- Carmen Clapp and Gonzalo Martinez de la Escalera.Aquaporin-1: a novel promoter of tumor angiogenesisTRENDS in Endocrinology and Meatabolism. Vol. 17 No.1 January 2006
- Saadoun S, Papadopoulos MC, Hara-Chikuma M, Verkman AS. Impairment of angiogenesis and cell migration by targeted aquaporin-1 gene disruption.Nature. 2005 Apr 7;434(7034):786-92.
- Carmen Clapp and Gonzalo Martinez de la Escalera.Aquaporin-1: a novel promoter of tumor angiogenesisTRENDS in Endocrinology and Meatabolism. Vol. 17 No.1 January 2006
- Saadoun S, Papadopoulos MC, Hara-Chikuma M, Verkman AS. Impairment of angiogenesis and cell migration by targeted aquaporin-1 gene disruption.Nature. 2005 Apr 7;434(7034):786-92.
- Rosengren S, Henson PM, Worthen GS.Migration-associated volume changes in neutrophils facilitate the migratory process in vitro.Am J Physiol. 1994 Dec;267(6 Pt 1):C1623-32.
- Rosengren S, Henson PM, Worthen GS.Migration-associated volume changes in neutrophils facilitate the migratory process in vitro.Am J Physiol. 1994 Dec;267(6 Pt 1):C1623-32
- Richard C, Gao J, Brown N, Reese J.Aquaporin water channel genes are differentially expressed and regulated by ovarian steroids during the periimplantation period in the mouse.
Endocrinology. 2003 Apr;144(4):1533-41.
- Rubanyi, G.M. et alEffecte of estrogen on endothelial function and angiogenesis
Vasc.Pharmacol 2002 38,89-98




Pingback:Lezioni di nefrologia, bilancio idrico, | GaiaMed